 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

三阴性乳腺癌多个创新治疗方法获批,生存期显著延长
【本文为疾病百科知识,仅供阅读】 2021-04-25 作者:厚朴方舟
乳腺癌是女性常见的恶性肿瘤,2020年的数据指出,乳腺癌发病人数已超过肺癌。三阴性乳腺癌(TNBC)是指雌激素受体(ER)、孕激素受体(PR)、人表皮生长因子受体2(HER-2)判定为阴性的乳腺癌,约占所有乳腺癌的10%~15%。与其他乳腺癌类型预后效果较好不同,三阴性乳腺癌侵袭性强,极易发生远处转移以及局部位置的复发,整体的5年生存率仅为77%[2](乳腺癌整体5年生存率为90%[3])。另外,三阴性乳腺癌的临床治疗选择十分有限,主要治疗方法为化疗,因此迫切需要更有效的治疗方案。随着靶向治疗和免疫治疗等新型治疗方法在癌症治疗中的应用,靶向治疗和免疫治疗在三阴性乳腺癌中也显现出良好的效果,显著延长了患者的生存期。
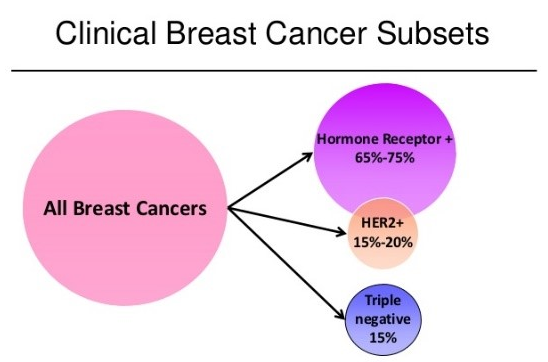
▲图源:komensandiego
头个提高三阴性乳腺癌无进展生存期和总生存期的治疗方法
4月7日,美国食品和药物管理局(FDA)已授予靶向抗癌药Trodelvy完全批准,用于治疗:先前已接受过至少2种治疗方法、其中至少1种治疗转移性疾病的不可切除性局部晚期或转移性三阴性乳腺癌(TNBC)成人患者。Trodelvy是头一个可提高三阴性乳腺癌患者无进展生存期(PFS)和总生存期(OS)的治疗方法,标志着三阴性乳腺癌治疗方面的一个重大进步。

▲图源:gilead
此次完全批准,基于3期ASCENT(NCT02574455)试验的结果,研究结果表明,与化疗相比,Trodelvy将无进展生存期显著延长(中位PFS:4.8个月 vs 1.7个月)、疾病进展或死亡风险显著降低57%、将总生存期显著延长(中位OS:11.8个月 vs 6.9个月)、死亡风险显著降低49%[4]。
头款三阴性乳腺癌免疫检查点抑制剂
2019年3月8日,FDA(美国食品和药物管理局)批准PD-L1单抗Atezolizumab(TECENTRIQ®)与紫杉醇结合蛋白的治疗方法,用于无法切除的局部晚期或具转移性,且肿瘤有明显的PD-L1表达的三阴性乳腺癌(TNBC)患者。Atezolizumab是全球头款用于治疗乳腺癌的免疫检查点抑制剂。
▲图源:FDA
此次批准基于IMpassion130(NCT02425891),研究结果表明,与对照组相比,Atezolizumab联合紫杉醇结合蛋白治疗,显著延长三阴性乳腺癌的无进展生存期(中位PFS:7.4个月vs4.8个月),将客观缓解率提高了20%(ORR:53%vs33%)。
Keytruda治疗三阴性乳腺癌效果显著
2020年11月,美国FDA已加速批准其重磅PD-1抑制剂Keytruda与化疗联用,用于经FDA批准的检测确定肿瘤表达PD-L1([CPS]≥10)的不可切除局部复发性或转移性三阴性乳腺癌(TNBC)患者。
▲图源:businesswire
此次加速批准是基于名为KEYNOTE-355的3期临床试验的结果,研究结果显示,Keytruda组与对照组相比,将疾病进展和死亡风险降低35%;无进展生存期显著延长(中位PFS:9.7个月vs5.6个月);缓解时间显著延长(中位DOR:19.3个月vs7.3个月)[6]。
除了与化疗联用可显著提高三阴性乳腺癌治疗的效果外,Keytruda单药作为手术后辅助治疗早期三阴性乳腺癌、单药治疗局部晚期或转移性三阴性乳腺癌均显现出良好的效果。
今年4月1日,Keytruda治疗接受过一线或二线系统治疗的三阴性乳腺癌患者的研究结果(KEYNOTE-119)发表在《柳叶刀·肿瘤》杂志上。研究结果显示,随着PD-L1表达水平的上升,化疗联用Keytruda的方案治疗的效果增强。在PD-L1 CPS≥10的TNBC患者群体中,Keytruda联合化疗显著延长了患者无进展生存期(中位PFS:9.7个月vs5.6个月)[7]。

▲图源:thelancet
另外,2020年2月发表在《The New England Journal of Medicine(NEJM)》的一项研究指出,Pembrolizumab联合化疗在未经治疗的Ⅱ期或Ⅲ期三阴性乳腺癌显现出良好的效果,完全缓解率比对照组高13.6%(64.8%vs51.2%)[8]。
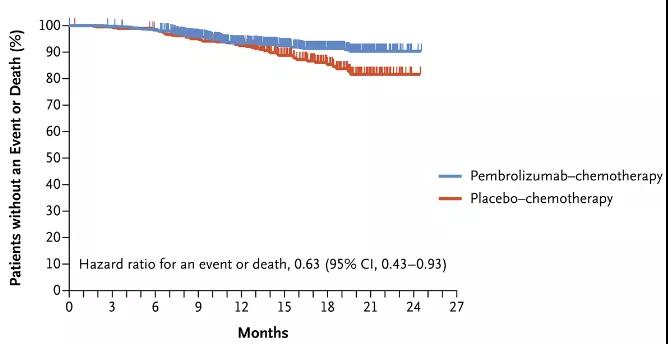
▲图源:NEJM
虽然三阴性乳腺癌的病情十分凶险,但研究人员还是在努力发掘抑制它的方法,目前已有不少成果披露,显著延长了患者的生存期。所以对于乳腺癌患者而言,积极的配合治疗,不主动放弃,才会出现各种新的可能。如希望了解更多有关三阴性乳腺癌治疗方案,可拨打热线400-086-8008联系我们。
参考来源:
[1] 世界卫生组织国际癌症研究机构
https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
[2] Triple Negative Breast Cancer Outlook: Survival Rates
https://www.healthline.com/health/triple-negative-breast-cancer-outlook-survival-rates-stage#survival-rates
[3] Survival Rates for Breast Cancer
https://www.cancer.org/cancer/breast-cancer/understanding-a-breast-cancer-diagnosis/breast-cancer-survival-rates.html
[4] FDA Approves Trodelvy®, the First Treatment for Metastatic Triple-Negative Breast Cancer Shown to Improve Progression-Free Survival and Overall Survival
[5] FDA approves atezolizumab for PD-L1 positive unresectable locally advanced or metastatic triple-negative breast cancer
[6] FDA Approves Merck’s KEYTRUDA® (pembrolizumab) in Combination With Chemotherapy for Patients With Locally Recurrent Unresectable or Metastatic Triple‑Negative Breast Cancer Whose Tumors Express PD-L1 (CPS ≥10)
[7] Pembrolizumab versus investigator-choice chemotherapy for metastatic triple-negative breast cancer (KEYNOTE-119): a randomised, open-label, phase 3 trial
[8] Pembrolizumab for Early Triple-Negative Breast Cancer
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号