 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

美国FDA批准TECENTRIQ的“小伙伴”诊断肺癌
【本文为疾病百科知识,仅供阅读】 2016-10-31 作者:厚朴方舟
据海外医疗服务机构厚朴方舟获悉,罗氏公司宣布美国FDA批准了其诊断性试剂盒VENTANA PD-L1(SP142)作为补充诊断,以鉴定治疗经治转移性非小细胞肺癌(NSCLC)患者的PD-L1表达水平,这些病人考虑使用肿瘤免疫治疗方法方法TECENTRIQ(atezolizumab)。
2016年5月18日PD-L1单抗atezolizumab获美国FDA批准用于治疗尿路上皮癌(UC),FDA同时还批准了TECENTRIQ的上述这款辅助诊断VENTANA PD-L1(SP142)分析试剂盒,用于测定肿瘤浸润免疫细胞PD-L1表达水平,便以帮助临床医师判断能从atezolizumab治疗获得更大获益的患者。
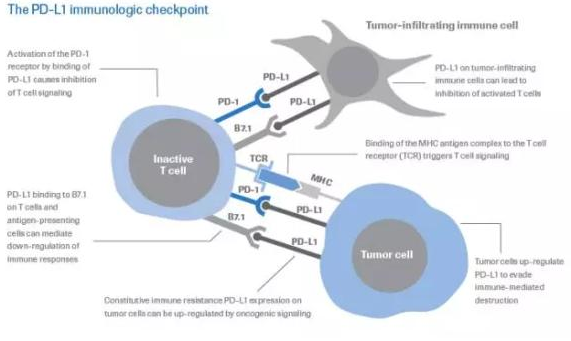
肺癌是癌症死亡的主要原因之一,每年估计占所有新增癌症病例的12.9%,在全世界约有159万人因此而死亡。同时,因为肺癌引发的死亡人数约占所有癌症相关死亡总数的五分之一。NSCLC是两种主要类型的肺癌之一,大约占所有肺癌病例的85%。在过去三十年中,与其他癌症相比,肺癌的生存率改善较小。近年来,靶向PD-1/PD-L1这一免疫检查点的治疗方案在治疗肺癌等一系列难治癌症方面取得可喜进展。
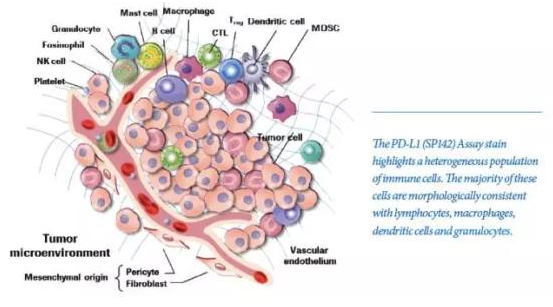
PD-L1表达量的诊断性试剂盒。确定患者的PD-L1表达水平可以提高对通过TECENTRIQ治疗可进一步获得的生存效益的了解。VENTANA PD-L1(SP142)测试是一种定性类型的免疫组织化学检测,使用兔源单克隆抗PD-L1的SP142抗体,用于评估使用福尔马林固定、石蜡包埋了(FFPE)的UC和NSCLC组织。PD-L1状态的确定具有指示特异性,基于任何强度的PD-L1表达肿瘤浸润性免疫细胞占据的肿瘤面积的比例(%IC)或表达PD-L1的肿瘤细胞的百分比(%TC)。
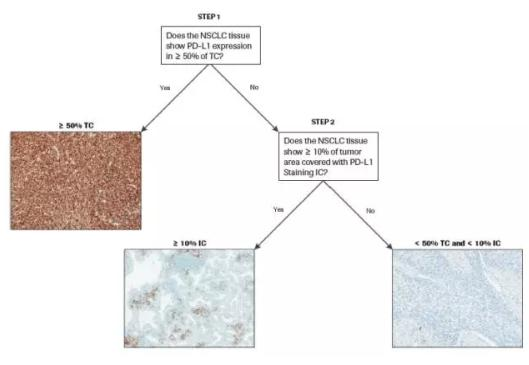
在一项TECENTRIQ的非随机研究中,通过VENTANA PD-L1(SP142)测定的尿路上皮癌组织中≥5%IC的PD-L1表达与增加的客观反应率(ORR)相关。
在NSCLC组织中的,通过VENTANA PD-L1(SP142)测定的≥50%TC或≥10%IC的PD-L1表达可能与源于TECENTRIQ治疗而增强的总体存活(OS)相关。本产品适用于体外诊断(IVD)使用。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
热门服务
推荐阅读
美国权威医学专家
美国医院排名
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号