 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

治疗NTRK融合阳性肿瘤,FDA加速批准广谱抗癌药Rozlytrek上市
【本文为疾病百科知识,仅供阅读】 2019-08-16 作者:厚朴方舟
美国时间8月15日,食品和药物管理局(FDA)宣布,加速批准罗氏(Roche)开发的Rozlytrek(entrectinib恩曲替尼)上市,用于治疗携带NTRK基因融合的成年和青少年癌症患者。在此之前,这类癌症患者还没有其它有效治疗方案。并且之前Rozlytrek已经获得了FDA的优先审查、突破性治疗和孤儿药认定。

这是继Keytruda和Vitrakvi之后,FDA批准的第三款“不限癌种”的抗癌治疗方法。它们靶向驱动癌症的特定基因特征,而不是肿瘤起源的组织类型。与此同时FDA还批准Rozlytrek治疗携带ROS1基因突变的非小细胞肺癌患者(NSCLC)。今年6月Rozlytrek已经在日本获批上市,治疗NTRK基因融合的实体瘤患者。
这一批准是基于多项临床试验的结果,其中包括名为STARTRK-2的关键性2期临床试验,名为STARTRK-1和ALKA-372-001的1期临床试验。在研究了54名患有NTRK融合阳性肿瘤的成人的四项临床试验中,研究人员评估了Rozlytrek缩小肿瘤的能力。
对这些试验数据的汇总分析表明,在NTRK融合阳性实体瘤患者中,Rozlytrek达到57.4%的客观缓解率(ORR),中位缓解持续时间(DOR)达到10.4个月。多达10种不同类型的实体瘤患者对这一治疗方法产生响应。
值得注意的是,对于肿瘤转移到大脑的实体瘤患者,Rozlytrek也能达到54.5%的颅内客观缓解率,获得缓解的患者中四分之一达到完全缓解。
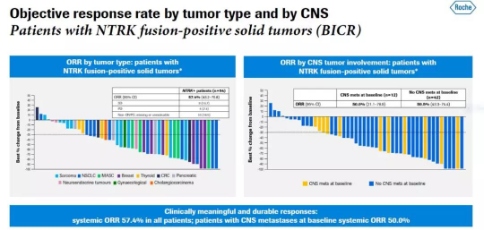
▲Rozlytrek针对NTRK融合阳性患者的效果结果(图片来源:参考资料[3])
FDA今天同时批准Rozlytrek用于治疗携带ROS1基因突变的转移性非小细胞肺癌患者(NSCLC)。临床试验结果表明,在51名ROS1阳性NSCLC患者中,总缓解率达到78%,完全缓解率达到5.9%。在肿瘤缩小的40名患者中,55%患者的缓解持续时间超过12个月。
关于Rozlytrek
Rozlytrek的活性药物成分为entrectinib(恩曲替尼),这是一种口服、选择性酪氨酸激酶抑制剂(TKI),靶向治疗携带NTRK1/2/3(编码TRKA/TRKB/TRKC)或ROS1基因融合的局部晚期或转移性实体瘤。Entrectinib可穿越血脑屏障,阻断TRKA/B/C和ROS1蛋白的激酶活性,较终导致携带ROS1或NTRK基因融合的癌细胞死亡。
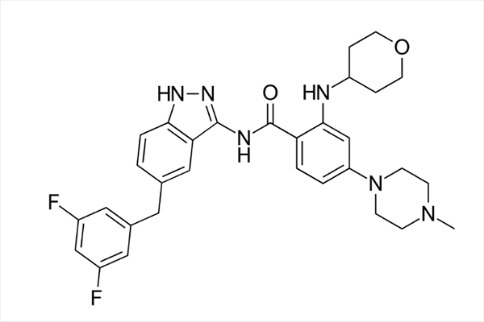
▲Rozlytrek分子结构式(图片来源:Ed (Edgar181) [Public domain])
Entrectinib针对原发性和转移性CNS疾病均具有效果,并且没有不良的脱靶活性。目前,罗氏正在调查entrectinib治疗多种实体瘤的潜力,包括NSCLC、胰腺癌、肉瘤、甲状腺癌、涎腺癌、胃肠道间质瘤和未知原发癌(CUP)。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:治疗过度嗜睡,“first-in-class”发作性睡病新药获美FDA批准 下一篇:又一孤儿药获批!多发性骨髓瘤患者治疗的新希望
热门服务
推荐阅读
美国权威医学专家
美国医院排名
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号