 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

首页 > 医疗前沿资讯 > 海外治疗指南 > BMS、强生丙肝新药有望率先在中国上市
BMS、强生丙肝新药有望率先在中国上市
【本文为疾病百科知识,仅供阅读】 2016-11-14 作者:厚朴方舟
据海外医疗领导品牌厚朴方舟了解,CFDA11月4日公布了第4批临床试验数据自查核查药品清单,包括奥希替尼片(AZD9291)、来迪派韦索磷布韦片(Harvoni)、盐酸达拉他韦片(Daklinza)在内的一大波外企重磅新药赫然在列。
由于这些品种被纳入自查核查受理号前4位字母是以“L”结尾,曾有网友对此迷惑不解。核查清单中出现的前4位字母以L结尾的受理号,所涉及的药品也都是在中国开展过国际多中心临床试验的。所以,这些受理号涉及的品种在通过临床数据核查后不是批准上市,而是拿到IND批件,同意免临床,再直接申报NDA,它们距离上市还是隔着一道报产程序的。
话音还未落,我们就欣喜地看到已经有相关品种报产。

由此也可以管窥到丙肝新药在中国注册申报所享受到的优待。
4月18日,CDE发布今年第3张优先审评公告,专门针对丙肝药物,强生和BMS的品种都在优先审评之列。
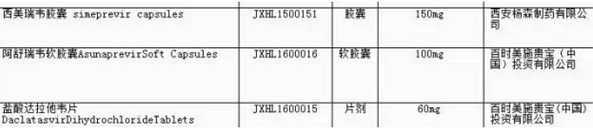
11月4日,CFDA发布第4张药品临床自查核查清单,上述3个受理号在列。
到如今,BMS、强生的丙肝新药已经纷纷报产,有望率先在中国上市,这对国内丙肝患者算是一个好消息,相信Gilead、AbbVie丙肝新药的上市申请也会马上出现在CDE承办目录里。
全球丙肝市场在猛烈爆发后开始萎缩,Harvoni、Sovaldi、Viekira、Daklinza(达拉他韦)+Sunvepra(阿舒瑞韦)、Olysio(西美瑞韦)的销售额都开始下滑。
中国是潜在的丙肝大市场,患者数量庞大,但患者诊断率低、支付能力差也是无法回避的问题。中国丙肝市场就像海上漂泊已久的船员远远眺望到的一个绿岛,现在终于触手可及了,但是只有真得上岸以后,才能真切体会到岛上的生存环境。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:欧盟批准辉瑞乳腺癌药物Ibrance一线/二线治疗HR+/HER2-转移性乳腺癌 下一篇:AbbVie在研泛基因型丙肝新药效果高达97.5%
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号