 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

首页 > 医疗前沿资讯 > 海外治疗指南 > 癌细胞转移重要机制有望成为药物新靶点
癌细胞转移重要机制有望成为药物新靶点
【本文为疾病百科知识,仅供阅读】 2016-06-29 作者:厚朴方舟
当人们发现癌症疾病就应该及时的治疗,治疗起来还比较容易。一旦癌细胞发生了转移就会很难治疗,甚至会给患者带来生命危险。当脱离了原有的肿瘤后,游离的癌细胞在获得了“自由”的同时,也离开了由其周边的癌细胞和细胞因子等组成的肿瘤微环境,从而失去该微环境所提供的保护作用。然而,当游离在体液中时,这些癌细胞更易受到攻击,因此有着较高的死亡率。尽管如此,还是有一些这样的癌细胞存活了下来,并且在身体的其他地方生成了新的病灶。那么,这些幸存的癌细胞是否有着一些特殊的生存能力呢?还是仅仅因为幸运便存活了下来?
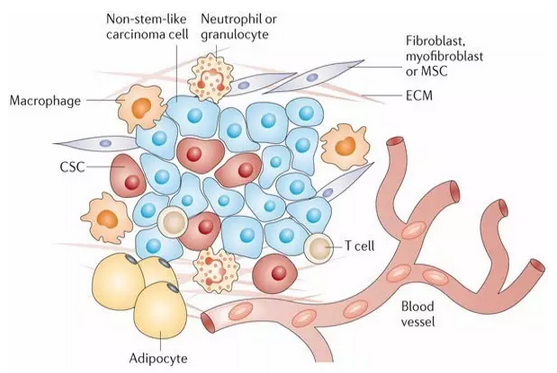
据出国看病服务机构厚朴方舟了解到,伦敦玛丽女王大学(QMUL)的科学院发现,这些异常顽强的癌细胞中原来存在着一种非同寻常的存活机制,使其具备向全身扩散的能力。这一发现将有望为癌症转移和继发性肿瘤发生提供更为有效的应对思路。
科学家们以位于细胞培养物、小鼠或斑马鱼体内的肿瘤为研究对象,分析了当癌细胞脱离肿瘤时内部发生的变化,并发现了一种维持此时癌细胞存活的新型分子机制。其中,整合素和受体酪氨酸激酶(RTK)是关键的组分。
整合素是一种位于细胞表面的蛋白,介导细胞与其外部基质的粘连和相互作用。整合素介导的跨膜信号传递维系着肿瘤中的癌细胞与其周围微环境的联系,对癌细胞的存活至关重要。正因为如此,对整合素功能进行有效阻断成为了抗癌药物开发的一大思路。然而,至今尚未有任何整合素抑制剂药物被批准用于癌症的治疗。而本研究的发现则可能对此给出合理解释,其原因也许就在于整合素在癌细胞转移时发生了“角色转换”,使得仅能作用于位于细胞表面整合素分子的抑制剂药物在此时变得无能为力。
原来,当癌细胞脱离了肿瘤后,整合素的角色就会发生很大的改变。这时,β1整合素会与另一个细胞膜上蛋白c-MET蛋白(RTK的一种)结合,然后一起进入细胞质内部,并结合到LC3B阳性的自噬相关内膜(autophagy-related endomembrane)上。不过,β1整合素和c-MET蛋白在那里并没有启动自噬作用,而是共同导致了ERK1/2激酶的持续磷酸化,从而激活其下游信号通路。这一信号通路的激活会对整个癌细胞产生影响,使其在没有与外界基质粘连的情况下,得以继续存活和生长,并具有生成肿瘤、侵袭和扩散的能力。
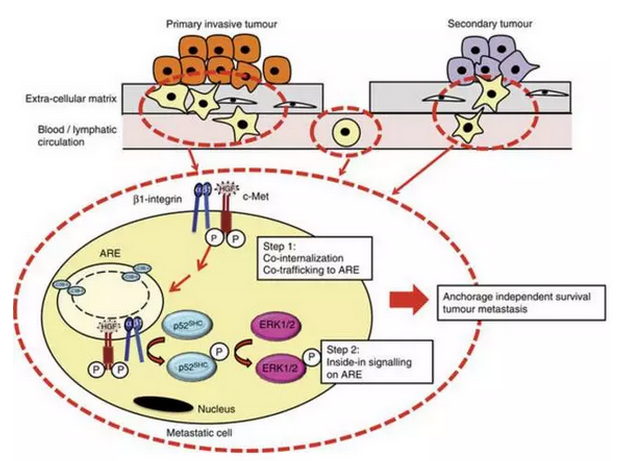
不仅如此,在针对源自乳腺和肺部的癌细胞的体外实验中,当研究者阻断了β1整合素和c-MET蛋白共同向细胞质内部转移的过程时,上述两类癌细胞便不再能够发生转移了。这说明,β1整合素和c-MET蛋白有望成为新的抗癌药物靶点,用于直接抑制癌细胞的转移过程。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号