 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

首页 > 医疗前沿资讯 > 海外前沿药物 > 2021年3月肿瘤领域获批新药汇总
2021年3月肿瘤领域获批新药汇总
【本文为疾病百科知识,仅供阅读】 2021-04-08 作者:厚朴方舟
肿瘤已成为造成死亡的第二大因素,如何治疗肿瘤患者是目前我国医疗相关人员,乃至世界人员面临的重大挑战。三月,万象更新,在肿瘤治疗领域,三月份也取得了重大的进展,不少重磅药物获批上市。厚朴方舟为大家整理了三月份肿瘤治疗领域获批的新药,希望能为大家提供些许帮助。
国内获批的肿瘤药物汇总
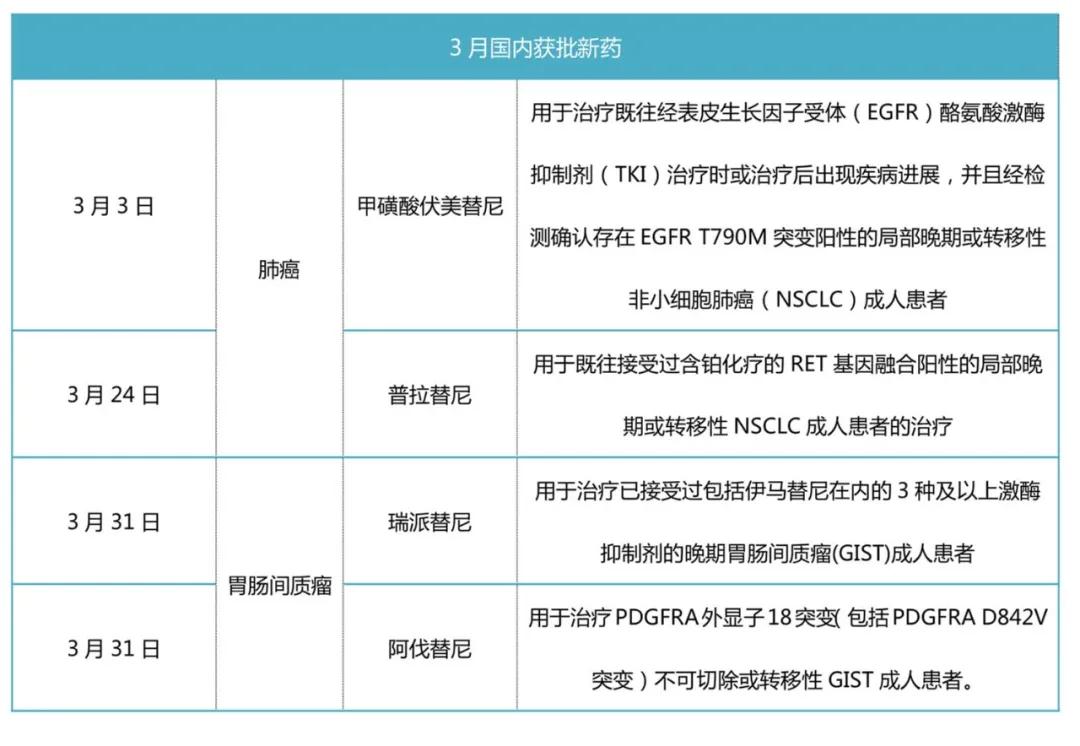
▲制图:厚朴方舟
详细数据:
1.甲磺酸伏美替尼
2020年美国临床肿瘤学会(ASCO)年会上的新研究数据显示伏美替尼治疗EGFR T790M突变阳性局部晚期或转移性非小细胞肺癌(NSCLC)的肿瘤客观缓解率(ORR)为74.1%,疾病控制率(DCR) 为93.6%,无疾病进展生存期(PFS)为9.6个月, 而且对于预后生存不佳的脑转移NSCLC也显示较强的效果[1]。
2. 普拉替尼
普拉替尼是国内率先获批的RET抑制剂。2020年世界肺癌大会(WCLC)上公布的新研究数据显示,普拉替尼在经含铂化疗的RET融合阳性非小细胞肺癌(NSCLC)中国患者中显示出了优越和持久的抗肿瘤活性,客观缓解率(ORR)为56%,安全性及耐受性良好,未出现与普拉替尼相关的不良事件导致的治疗终止或死亡[2]。
3.瑞派替尼
瑞派替尼的获批主要基于INVICTUS研究数据。结果显示,瑞派替尼治疗晚期胃肠间质瘤(GIST)具有显著的无进展生存期获益和广泛的安全性:瑞派替尼组中位无疾病进展生存期(PFS)为6.3个月,安慰剂组为1.0个月,显著降低了84%的疾病进展风险; 瑞派替尼组客观缓解率为11.8%,安慰剂为0.0%[3]。
4.阿伐替尼
阿伐替尼是中国率先获批的针对PDGFRA外显子18突变型胃肠间质瘤(GIST)的精准治疗药物。研究数据表明,阿伐替尼在携带PDGFRA D842V 突变的中国GIST患者中初步显示出了显著的抗肿瘤活性,总体客观缓解率(ORR)为62.5%[4]。
国外获批的肿瘤药物汇总
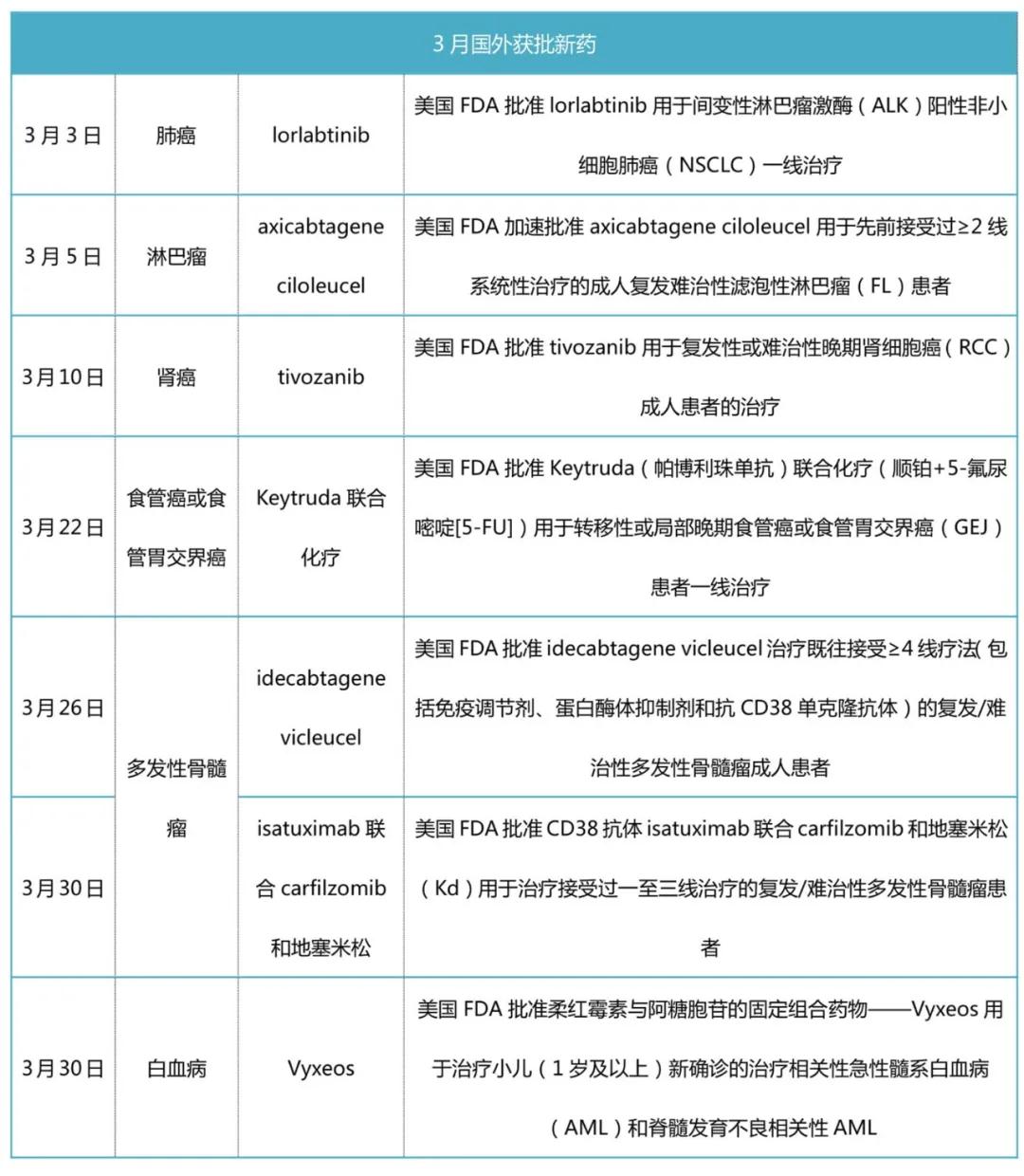
▲制图:厚朴方舟
详细数据:
1. Lorlabtinib
发表在《新英格兰医学杂志》中的研究数据指出,在既往未经治疗的晚期ALK阳性非小细胞肺癌(NSCLC)患者中,与克唑替尼相比,lorlabtinib显著提高了患者的无疾病进展生存期(PFS),将疾病进展或死亡风险降低了72%[5]。
2.axicabtagene ciloleucel
axicabtagene ciloleucel(Yescarta)是率先被批准用于治疗惰性复发难治性滤泡性淋巴瘤(FL)的CAR-T治疗,此次获批主要基于ZUMA-5研究数据,结果显示,复发难治性滤泡性淋巴瘤(FL)患者经axicabtagene ciloleucel治疗后,总体客观缓解率(ORR)达到91%,完全缓解(CR)率为60%;研究中患者的1年持续缓解率为76.2%[6]。
3.Tivozanib
III期TIVO-3研究结果显示,与索拉非尼相比,tivozanib可明显改善复发性或难治性肾细胞癌患者的无疾病进展生存期(PFS),Tivozanib组和索拉非尼组的中位PFS分别为5.6个月和3.9个月[7]。
4.Keytruda联合化疗
此次获批基于关键III期KEYNOTE-590试验数据,临床结果显示,与化疗相比,Keytruda联合化疗显著延长了食管癌患者总生存期(中位OS:12.4个月 vs 9.8个月);降低了27%的死亡风险;无进展生存期显著延长(中位PFS:6.3个月 vs 5.8个月);疾病进展或死亡风险降低35%。另外,在Keytruda联合化疗组的缓解率也明显高于化疗组(ORR:45.0% vs 29.3%),疾病缓解持续时间有效延长(中位DOR:8.3个月 vs 6.0个月)[8]。
5. idecabtagene vicleucel
idecabtagene vicleucel(Abecma)是靶向BCMA的CAR-T治疗,也是FDA批准的初个针对多发性骨髓瘤的基于细胞的基因治疗。研究结果显示,客观缓解率(ORR)为72%,完全缓解(CR)率为28%。据估计,达到完全缓解患者中有65%的患者的缓解状态持续了12个月[9]。
6. isatuximab联合carfilzomib和地塞米松
isatuximab联合carfilzomib和地塞米松在复发/难治性多发性骨髓瘤治疗领域显现出良好的效果。此次获批主要基于III期临床试验IKEMA研究的结果,结果显示,与标准Kd(carfilzomib联合地塞米松)治疗相比,isatuximab联合Kd可将疾病进展或死亡风险降低45%[10]。
7. Vyxeos
此次批准主要基于关键3期研究CPX351-301,研究结果显示,与标准的阿糖胞苷+柔红霉素(7+3)化疗方案相比,Vyxeos治疗急性髓系白血病(AML)和脊髓发育不良相关性AML总生存期(OS)显著改善(中位OS:9.6个月 vs 5.9个月)、完全缓解率显著提高(37% vs 26%)、造血干细胞移植(HSCT)率提高(34% vs 25%)[11]。
未来,研究人员将继续深耕肿瘤领域,研发出更多创新的药物,造福世界肿瘤患者。厚朴方舟作为国内知名海外医疗服务机构,可以帮助肿瘤患者了解更多肿瘤资讯、预约世界名医确定理想的治疗方案,并提供一站式出国看病服务及远程会诊服务,了解更多肿瘤治疗药物可拨打热线400-086-8008联系我们。
参考来源:
[1] http://cn.lillyasiaventures.com/blog/egfr-tki
[2] http://news.bioon.com/article/6783529.html
[3]http://caifuhao.eastmoney.com/news/20210331171837759815680
[4]https://www.jiemian.com/article/5892845.html
[5]FDA Approves Lorlatinib for Metastatic ALK-Positive NSCLC
[6]U.S. FDA approves Yescarta® for Relapsed or Refractory Follicular Lymphoma After Two or More Lines of Systemic Therapy
[7]AVEO Oncology Announces U.S. FDA approval of FOTIVDA® (tivozanib) for the Treatment of Adult Patients with Relapsed or Refractory Advanced Renal Cell Carcinoma
[8]FDA Approves Pembrolizumab for Esophageal or GEJ Carcinoma
[9]BMS, bluebird's CAR-T Abecma wins FDA approval for multiple myeloma
[10]FDA approves isatuximab-irfc for multiple myeloma
[11]Jazz Pharmaceuticals Announces FDA approval of Additional Indication for Vyxeos (daunorubicin and cytarabine) for the Treatment of Secondary Acute Myeloid Leukemia in Pediatric Patients - FirstWord Pharma
来源:医脉通肿瘤科
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:Lumoxiti获批用于毛细胞白血病,显著提高疾病缓解率 下一篇:多个晚期胃癌靶向治疗药物获批,胃癌治疗开启精准医疗时代
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号