 全球服务热线:400-086-8008
全球服务热线:400-086-8008- 日本语
 全球服务热线:400-086-8008
全球服务热线:400-086-8008

国际医药巨头PD-1抑制剂研究获得新突破且有上市
【本文为疾病百科知识,仅供阅读】 2015-09-06 作者:厚朴方舟
据国内大出国看病服务机构-厚朴方舟了解,经过了短暂但显著有效的临床试验,备受瞩目及希望的(PD1)抑制剂赫然被批准进入美国或日本药品市场,所以我们应该对这些药品拭目以待。中国患者目前想获得这些药物使用,较简单的办法就是出国看病。
PD-1单克隆抗体一直都是免疫治疗方法方法的热点,也是医药巨头竞争的前沿阵地。近年来,国外陆续有PD-1类产品上市,投资者都给予了很高的期望。2014年较热门的抗体是百时美施贵宝的纳武单抗和默沙东的Keytruda,主要用于治疗黑色素瘤,其中EvaluatePharma给出纳武单抗的2020年市场销售预期在62.01亿美元,而Keytruda的全球销售将在2020年达到39.22亿美元.
近两年来,美国临床肿瘤年会较令人兴奋的临床试验,大概就是PD-1抗癌抗体带来的黑色旋风。PD-1抗体带来的临床抗癌效果是前所未有的。它可以控制50%的皮肤癌病人的癌症进展,痊愈10%左右的皮肤癌病人。对于顽固的非小细胞肺癌病人,多年来医学上束手无策,PD-1抗体也对24%的病人有临床控制效果。由于其广谱抗癌作用,对肾癌,胃癌,乳腺癌,膀胱癌,血癌,头颈癌、肠癌和脑瘤等癌症的临床效果也正在临床二期或三期试验之中。
2012年6月28号《新英格兰医学杂志》年发表的纳武单抗针对各种癌症(非小,黑色素瘤,RCC)的临床试验结果,测试了三种纳武单抗的治疗浓度:1mg/kg,3mg/kg和10mg/kg,包括129名非小细胞肺癌的患者(之前都接受过多次各种治疗),ORR是17%(统计所有三种浓度)。
2014年百时美施贵宝的PD1抑制剂nivolumab率先在日本上市,用于治疗晚期黑色素瘤。目前也计划向FDA提交上市申请。此外,nivolumab也打算同时向FDA提交非小细胞癌适应症的上市申请,而其治疗肾细胞癌的三期临床也在进行中。
2014年9月4日,美国FDA批准默克公司的pembrolizumab用于治疗晚期或无法手术切除的对其他药物无响应的黑色素瘤。支持此次获批的是一项基于173例黑色素瘤患者的非对照I期临床试验,在这个试验中pembrolizumab使24%黑色素瘤患者体内的肿瘤大小出现缩小,效果至少持续1.4-8.5个月。
2015年罗氏和阿斯利康研究的PD1抑制剂产品也已经进入三期临床,主要治疗肺小细胞型肺癌。
目前上市及处于临床阶段的PD-1或PD-L1抑制剂
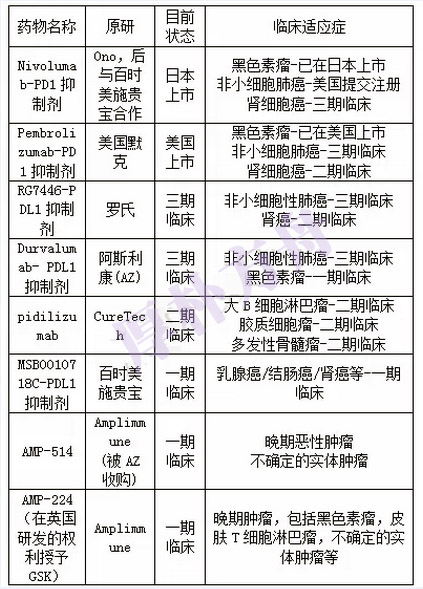
日本和美国的PD-1临床对患者的要求
患者在初次用药7日前检查结果应满足以下基准:白细胞数2000/mm³以上且中性粒细胞数1500/mm³以上;血小板数100000/ mm³以上;血红蛋白在9.0g/DL以上;AST(GOT)以及ALT(GPT)在设施正常值上限3.0倍以下;总胆红素在设施正常值上限2.0倍以下;肌酸酐在2.0mg/DL以下。另外,排除标准中明确规定了自身免疫病患者、移植患者和HBV/HCV检测阳性的患者不能入组。
厚朴方舟海外医学专家指出,PD-1抗体对各种癌症的效果是很好的,但不是所有患者都会对PD-1有响应。 目前来看,恶性黑色素瘤患者中的30%-40%可以从PD-1抗体治疗中获益,非小细胞肺癌的响应比例大概是20%,肝癌的初步数据也是20%,肾细胞癌的大概是20%到30%。如果能够提前预测它的效果,对患者来说 是大功一件,既能避免在PD-1抗体上浪费时间,又能避免不必要的经济损失。
厚朴方舟2012年进入海外医疗领域,总部位于北京,建立了由全球权威医学专家组成的美日名医集团,初个拥有日本政府官方颁发的海外医疗资格的企业。如果您有海外就医的需要,请拨打免费热线400-086-8008进行咨询!
本文由厚朴方舟编译,版权归厚朴方舟所有,转载或引用本网版权所有之内容须注明"转自厚朴方舟官网(www.hopenoah.com)"字样,对不遵守本声明或其他违法、恶意使用本网内容者,本网保留追究其法律责任的权利。
上一篇:治疗慢性丙型肝炎方案:达卡他韦Daclatasvir受各国青睐 下一篇:施贵宝前列个对肺癌有效的PD-1药物纳武单抗大揭密
热门服务
推荐阅读
日本权威医学专家
日本医院排名
服务案例更多>
 全球咨询服务热线
全球咨询服务热线
400-086-8008

English | 微信端

互联网药品信息服务资格证书编号:(京)·非经营性·2015·0179
厚朴方舟健康管理(北京)有限公司 版权所有 www.hopenoah.com
京ICP备15061794号
京公网安备 11010502027115号